7 概述
腦室-腹腔分流術是把一組帶單向閥門的分流裝置置入體內,將腦脊液從腦室分流到腹腔中吸收。簡稱V-P手術。Kausch於1905年首次開展這種手術,但當時不被人們重視,到了1955年Jackson報告62例這類手術,有一定效果。而腦室-心房分流術也有不少缺點,嚴重者可導致病兒死亡。因此,腦室-腹腔分流術又重新受到重視,使用日益廣泛。
12 手術步驟
12.1 1.頭皮弧形切口
作在右耳輪上後4~5cm處,顱骨鑽孔的大小與貯液器底座相當。切開硬腦膜,將腦室導管前端送到腦室前角。導管在適當長度剪斷並接於貯液器接頭上。將貯液器置於骨孔內與骨膜縫合固定,再將閥門近端連接在貯液器出口上,注意閥門上下方向不能顛倒,閥門泵室上的箭頭指向腦脊液分流的方向。
12.2 2.分離皮下隧道
腹腔導管是從頭部切口經頂顳部、耳後、頸部、胸部到達上腹部。皮下隧道較長,可分2~3次打通。第1個切口在乳突下方,第2個切口在鎖骨下,第3個切口在右上腹劍突下。用鈍頭金屬導子,分段通過皮下深層分離,製成一皮下隧道。
12.3 3.安裝腹腔導管
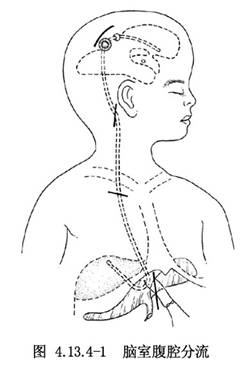
導管近端與閥門出口相接,遠端通過皮下隧道進入右上腹部切口。導管在頸部最好有一弧形彎曲,以便頸部活動時伸展。腹腔導管末端放置的常用位置有二:①腹腔管置於肝臟膈面。在腹部劍突下,做旁正中切口或正中切口,長5cm左右。按層切開腹壁、腹膜後,暴露肝臟左葉,將腹腔導管末端放置於肝臟膈面之上。導管在腹腔內長度約10cm,最好選用末端側壁上有4個裂隙開口的導管,以防止逆流和管腔閉塞,並將導管縫在肝圓韌帶上,防止脫落。導管一旦脫落,離開肝臟膈面,遊離在腹腔內,極易被大網膜包裹而阻塞(圖4.13.4-1)。②腹腔管置於遊離腹腔內。腹部切口可在上腹部或下腹部中線或旁中線,長約3cm,最好避開闌尾炎切口。進入腹腔後,證實無腹膜粘連等疾病後,即可將導管末端送至腹腔內,導管末端最好有多個小圓孔開口,儘量遠離腹壁切口,也不可在腹膜切口附近盤曲,一般放入右(或左)側髂窩內。遊離於腹腔內的導管長度應達20~30cm以上,導管可在腹膜切口上縫合固定。
近年有人用腹腔鏡把導管末端放入小網膜囊內,可大大簡化手術,同時可以減少管端被大網膜堵塞和避免穿破腸管等危險。此外,有個別作者用套管穿刺法,利用帶有管芯的套管,在腹部旁正中穿破腹腔,拔出管芯後,把腹腔管從套管內插入腹腔,取出套管,固定導管後,將導管近端通過腹部-胸部-頸部皮下隧道,與頭部閥門管相接。
12.4 4.縫合
導管固定後,按層縫合腹膜與腹壁。
15 併發症
15.1 1.消化道症狀
病兒術後可能出現腹脹、腹痛、食慾下降或噁心嘔吐等症狀。發生原因除手術搔擾之外,主要是腦脊液對腹膜的刺激所致,一般一週左右可消失。
15.2 2.感染
由於分流導管皮下途徑長,局部感染機會較多,發生感染後可引起腦室炎、腦膜炎等顱內感染,也可引起腹膜炎、膈下膿腫或腹腔膿腫;局部皮下感染則出現皮下蜂窩組織炎或皮下膿腫。所以術中要嚴格消毒,術前、術後應用抗生素極爲重要。
15.3 3.分流導管障礙
發生的原因有:①閥門阻塞,多因腦室液蛋白過高,薄膜閥門中沉澱物積存所致。因此對腦室液蛋白超過1000mg/L時,不用閥門,僅用裂隙導管進行分流。腹腔導管末端的4個裂隙開口,用小刀切開,加長到1cm,以利分流。待腦室液蛋白含量下降後,改用正規閥門導管分流。②腹腔管扭曲,管端開口被大網膜包裹或形成假性囊腫(內含腦脊液),均可使分流失敗。發現後應及時處理,重新安置導管到腹腔其他部位,或改用其他分流術。
15.4 4.腹腔導管脫出
最常見的是導管自腹部切口脫出,部分乃至全部脫出腹腔,暴露於皮外。這是由於皮下隧道太淺,導管長期與表皮磨擦、壓迫,使皮膚壞死,或繼發感染,縫線脫落,導管脫出腹壁外。出現這種情況時,可根據切口情況處理。如切口無感染,肉芽比較新鮮,導管部分脫出者,可用抗生素溶液溼敷3天后,導管改道重新放入腹腔內,裂開的切口全層縫合,部分病人可以痊癒;如切口明顯感染,應立即更換新的腹腔管。
15.5 5.腹腔臟器損傷
有的腹腔導管末端質地堅硬,如Raimondi導管的管壁裝有不鏽鋼彈簧,由於手術創傷或導管末端長期機械摩擦,可能造成腸穿孔,橫膈穿孔和陰道穿孔。現在已有新型導管面市,管壁沒有金屬,主要由硅彈性橡膠製造,導管比較結實,不易發生導管壁機械性壓扁或扭曲,損傷內臟的機會也大大減少。